
同类最优的抗HIV药物:必妥维
重磅炸弹——同类最优的抗HIV药物:必妥维
1981年6月5日,美国疾病控制和预防中心(CDC)发表了一份《发病率和死亡率周报》(MMWR),其中描述了五例年轻、健康的男同性恋者的罕见肺部感染,卡氏肺囊虫肺炎(PCP)。
当时,人们还不知道到导致该病的发病原因。一年后,这种神秘的疾病有了一个名字:获得性免疫缺陷综合征,即艾滋病(AIDS),它破坏了免疫系统,使身体受到各种感染。
1983年,科学家终于发现了导致艾滋病的病毒,并将其命名为人类免疫缺陷病毒(HIV)。此后,研究人员开启了针对该病毒的抗病毒疗法。
然而,事实证明,艾滋病毒在体内很难被杀死。这是因为,HIV病毒攻击的目标是辅助T细胞,这些细胞通常是人体细胞免疫的主要功能细胞。如果T细胞被破坏的过多,那么人体对病毒和其他”机会性”感染将毫无抵抗力。并且,与导致感冒和流感的病毒不同,HIV是一种逆转录病毒,它们更擅长欺骗体内的宿主细胞,产生更多的拷贝,造成终身感染。
到1987年,仅在美国就有32000人感染了艾滋病毒,其中一半以上的人死亡。
在首次报告HIV后的第一个十年里,第一个抗艾滋病药物,齐多夫定(AZT)就上市了(1987年)。齐多夫定是1960年代被开发的一种失败的抗肿瘤药物。
齐多夫定在抗艾滋病方面的成功,可谓“失之东隅。收之桑榆”。齐多夫定通过阻断病毒逆转录酶来发挥作用,可以显著的延长艾滋病患者的生命。
在接下来的几年里,美国食品和药物管理局(FDA)批准了其他几种与AZT作用类似的药物,这些药物都属于核苷类逆转录酶抑制剂(NRTIs)。
然而,由于病毒变异,随着时间的推移,很多药物不再起作用了。到20世纪90年代初,HIV是25至44岁美国人的头号致死因素。因此,亟需新作用机制的抗病毒药物。
1995年,FDA批准了沙奎那韦,它是第一个获批的HIV蛋白酶抑制剂。一年后又出现了另一类抗逆转录病毒药物,称为非核苷类逆转录酶抑制剂(NNRTI),例如奈韦拉平(Viramune)。
这些药物为抗HIV综合治疗的新时代铺平了道路。医生们开始使用沙奎那韦加上AZT或其他抗逆转录病毒药物的处方。这种综合疗法被称为高活性抗逆转录病毒疗法(HAART),即“鸡尾酒”疗法。
“鸡尾酒”疗法在1996年成为HIV治疗的新标准。HAART大大延长了艾滋病患者的寿命。但是,HAART需要每天服用许多种药。多次服药和药物的副作用使许多人放弃了HIV治疗。这促使了复方单片的开发。
到1997年,FDA批准了批准了一种二合一片剂,名为卡贝滋(Combivir)的药片,它包含两种抗HIV药物,更容易服用。近年来,新的HIV药物类别不断涌现。今天,有30多种HIV药物可用。许多人每天只需吃一片药就能控制他们的艾滋病毒。
从 2021 年全球前十大 HIV 药品来看,销售额都在6亿美元以上,最高销售额的是吉利德于2018年推出的必妥维(Biktarvy, 比克恩丙诺),被认为是目前同类最优的抗逆转录病毒疗法(ART)+整合酶抑制剂为基础的鸡尾酒方案。
必妥维是一种完整的、单片的、一天一次的处方药,用于治疗体重成人和儿童的HIV-1病毒感染。它既可用于从未服用过HIV-1药物的人,也可用于正在更换现有HIV-1药物的人。
吉利德于2017年6月向美国FDA提交上市申请,于2018年2月获得美国FDA批准,其后陆续在欧盟、我国香港地区等全球多地获批。作为吉利德销售额最高的抗病毒产品之一,2021年,必妥维的销售额达到82.4亿美元,比2020年增长18.8%。
到2025年,预计全球销售额将达到100亿美元。
必妥维是一种三联复方单片制剂(BIC/FTC/TAF),活性成分包括比克替拉韦(BIC)/恩曲他滨(FTC)/丙酚替诺福韦(TAF)。其中,比克替拉韦(BIC)是FDA于2018年2月批准的一种新型整合酶链转移抑制剂(INSTI),适用于初治的艾滋病毒感染者(PLWH),以及在目前的ART上病毒学抑制至少3个月的PLWH,之前没有治疗失败史或对BIC单片疗法(STR)的任何成分的耐药性。
BIC已被证明能有效地抑制链式转移活性,其浓度与埃维他韦(EVG)和多鲁特韦(DTG)相似,但是,其独特的结构能最大限度地减少药物间的相互作用,增加蛋白质结合,并改善溶解度。
目前,BIC每天50毫克只能作为固定剂量与丙酚替诺福韦(TAF)每天25毫克和克恩曲他滨(FTC)每天200毫(BIC/FTC/TAF)的组合使用,即必妥维。
在两项研究关键的III期临床试验中,在全部240周,使用必妥维治疗的研究中,超过98%的参与者达到并保持了检测不到的病毒载量(HIV-1 RNA<50拷贝/毫升)。
第一个试验是Gallant等人在欧洲、拉丁美洲和北美进行了一项多中心非劣效研究(1489号试验),参与者(n=629)被随机分配到必妥维或共同配制多鲁特韦/阿巴卡韦/拉米夫定(50/600/300 mg,DTG/ABC/3TC),以及配套的安慰剂,每天一次,持续144周。
第二个III期随机对照临床试验(1490试验)是Sax等人在645名参与者中评估了必妥维与DTG+F/TAF相比的非劣效性试验。
临床研究结果显示,必妥维在不同的成人群体中均起作用。在第48周,92.4%(n=290/314)服用必妥维的患者和93.0%(n=293/315)服用ABC/DTG/3TC的患者达到了HIV-1 RNA<50 c/ml的主要终点。在1490研究中,共有645名未接受治疗的成年艾滋病患者被1:1随机分配到必妥维或DTG+FTC/TAF。在第48周,89.4%(n=286/320)服用必妥维的患者和92.9%(n=302/325)服用DTG+FTC/TAF的患者达到了HIV-1 RNA<50 c/ml的主要终点。
在随后的五年随访分析中,没有出现耐药性而导致的治疗失败,进一步证明了必妥维在治疗无效的成年人中治疗HIV-1的疗效和耐受性。
必妥维在临床研究发现的最常见的副作用是腹泻(6%)、恶心(6%)和头痛(5%)。
除此之外,也会出现一些严重的副作用,包括免疫系统的变化、肾脏问题,如肾衰竭、乳酸中毒等。如果患者出现虚弱或比平时更累,肌肉异常疼痛,气短或呼吸急促,胃痛并伴有恶心和呕吐,手脚冰凉或发青,感到头晕或头晕,或心跳加快或不正常,皮肤或眼睛的白色部分变黄,尿液呈深 “茶色”,大便呈浅色,连续几天或更长时间食欲不振,恶心,或胃区疼痛等症状时,需要及时就医。
回到市场方面,2020年全球约有3770万人感染了艾滋病毒,这对抗HIV药物提出了巨大需求。
根据弗若斯特沙利文的资料显示,全球HIV药物市场由2017年的325亿美元增长至2021年的380亿美元,复合年增长率为4.0%。
预计2025年将达到479亿美元及2030年将达到575亿美元,2021年至2025年的复合年增长率为6.0%,而2025年至2030年的复合年增长率为3.7%。
在中国,根据弗若斯特沙利文的资料显示,2021年感染HIV的人口达到150万人,预计2025年将达到170万人,2030年将达到210万人。
目前国内抗HIV用药市场规模在 30-40 亿元左右。患者基数增加、诊断率和治疗率提高、医保支付能力提升及自费人群的逐渐增加,将共同推动我国抗HIV用药市场规模的快速提升,预计2024年我国抗HIV药物市场规模将接近60亿元。
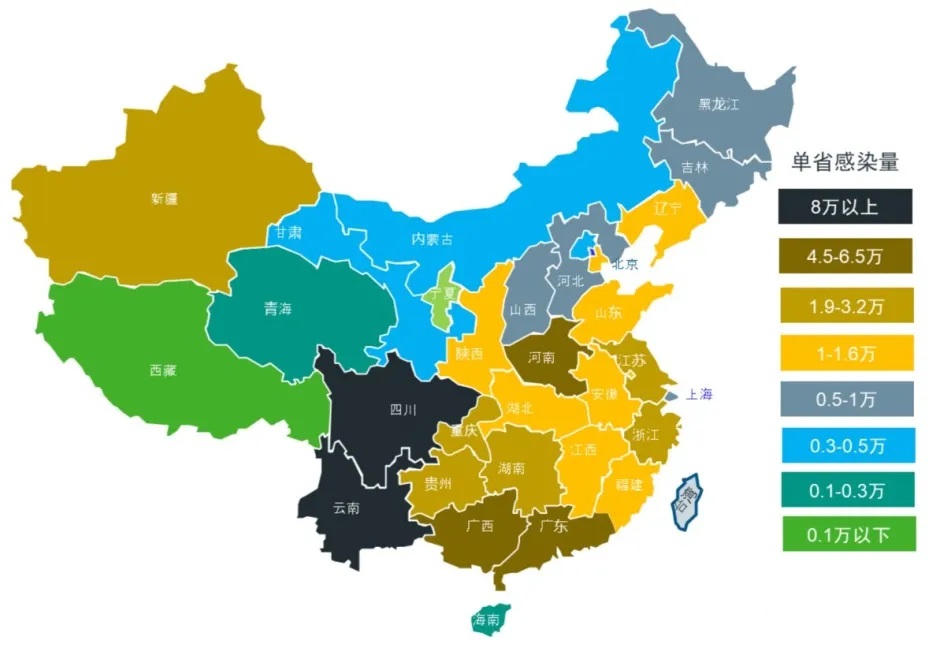
中国HIV感染人数地区分布
尽管发病人数、市场规模增长迅速,但是,目前中国市场上的大部分HIV药物为单剂抗逆转录病毒药物,而不是在发达市场更容易获得的含有多种ART制剂的复合药物。
国内HIV领域还缺乏国产创新药。目前国内已经上市的国产创新药物仅有3款:前沿生物的艾博卫泰(于2018年获批)、 艾迪药业的艾诺韦林(于2021年6月获批)、真实生物的阿兹夫定(于2021年7月获批、有条件上市)。
总体说来,我国抗HIV药物开发与发达国家相比,差距巨大,尤其缺乏复合、长效抗HIV药物。但是,考虑到经济水平,患者支付能力、医保政策等因素,相信未来抗HIV药物开发方面会迎来一场变革。
参考文献
https://www.webmd.com/hiv-aids/hiv-treatment-history
BIKTARVY:https://www.biktarvy.com/what-is-hiv
Tsiang M, Jones G S, Goldsmith J, et al. Antiviral activity of bictegravir (GS-9883), a novel potent HIV-1 integrase strand transfer inhibitor with an improved resistance profile[J]. Antimicrobial agents and chemotherapy, 2016, 60(12): 7086-7097.
Hill L, Smith S R, Karris M Y. Profile of bictegravir/emtricitabine/tenofovir alafenamide fixed dose combination and its potential in the treatment of HIV-1 infection: evidence to date[J]. HIV/AIDS (Auckland, NZ), 2018, 10: 203.
华安证券报告《拨云见月, HIV 抗病毒药物迭代推出》